在不锈钢的合金元素中,铬是最重要的元素。由于铬形成的致密、稳定的Cr2O3薄膜的保护,阻止了介质对金属基体的继续渗入腐蚀,所以,钢中如果含铬量达5%,就显示出一定的耐腐蚀作用。

但不是所有含铬的钢都可以作不锈钢使用,经过多年的研究和实践,人们发现,依据腐蚀的电化学理论,为了提高钢的电极电位,把铬加入到铁基固溶体中时,只有铬含量达到一定浓度,即当铬的原子比达到1/8、2/8、3/8、…n/8,铁基固溶体的电极电位才会跳跃式地增高,腐蚀也因此而减弱,钢的耐腐蚀性能才会明显地提高,见图1-2和图1-3。
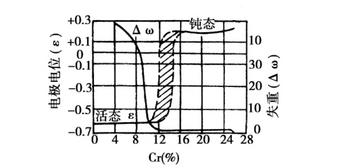
图1-2 铁-铬合金在1N的FeSO4溶液中与甘汞电极的比较电位以及在3N的HNO3中的腐蚀率
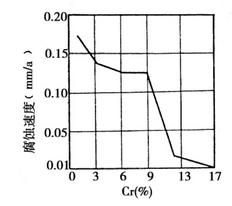
图1-3 铬钢在海水中的腐蚀速度与含铬量的关系
铬原子引起钢的电极电位第一次突变增高是铬占1/8原子比,即12.5%原子比时,如果折算成质量百分数则为:
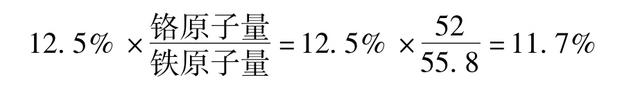
这个11.7%的铬含量就是构成不锈钢中的含铬量的最低界限,亦即钢中铬含量高于这个界限才可称为不锈钢。
当然,随着腐蚀介质条件的不同,有时钢中的铬含量还要提高,如在氧化性较强的介质中,铬含量要高于16%的钢才会有明显的钝化能力。工业中应用的不锈钢的铬含量一般在12%~30%。可以说,几乎没有一种不锈钢不含铬,所以说,铬是不锈钢中最重要的、起决定性作用的合金元素。













